编者按:2021年美国癌症研究协会(AACR)年会分别于2021年4月10-15日、5月17-21日在线举行。由复旦大学附属肿瘤医院开展的一项针对中国ER+/HER2-晚期乳腺癌的Ⅰ期剂量爬坡和剂量扩展试验入选大会壁报,研究初步结果显示FCN-437c安全性良好,毒性可耐受。《肿瘤瞭望》邀请该研究第一作者张剑教授对该研究进行介绍,以飨读者。
CT-117——CDK4/6抑制剂FCN-437c在中国ER+/HER2-晚期乳腺癌(ABC)女性患者中的Ⅰ期剂量爬坡和剂量扩展试验
研究背景:CDK4/6已被证实在细胞增殖中起着至关重要的作用,尤其在ER阳性的乳腺癌中经常出现失调。迄今为止,已有三种口服可生物利用的CDK4/6抑制剂palbociclib,ribociclib和abemaciclib获得批准上市,与芳香化酶抑制剂(AI)或氟维司群联合或单药治疗ER+/HER2-ABC。FCN-437c是第二代口服CDK4 / 6抑制剂,在体内模型中联合AI或氟维司群具有高效的抗肿瘤活性,良好的药代动力学(PK)特性和脑渗透性,以及可耐受的毒性。
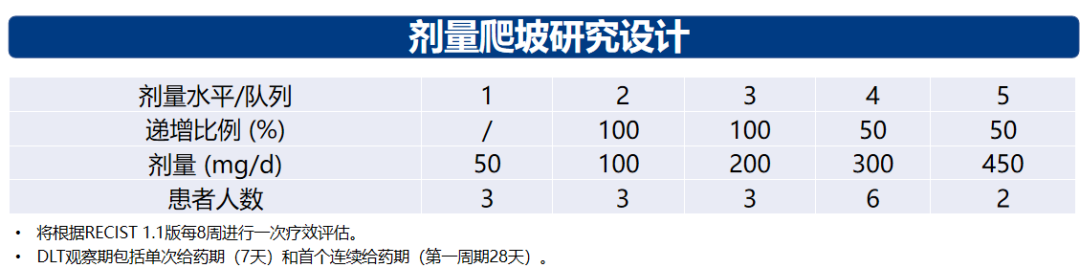
研究方法:本研究为开放、首次人体Ⅰ期试验,旨在评估FCN-437c单药在标准治疗失败的晚期乳腺癌患者(Ia期)以及联合来曲唑治疗一线晚期乳腺癌患者(Ib期)的安全性、最大耐受剂量(MTD)、药代动力学特性和抗肿瘤活性。在本摘要中,我们展示1a期研究结果。本研究遵循常规的3+3研究设计进行剂量爬坡试验,起始剂量为50 mg。给药3周后停药1周,28天为一周期。从2019年2月13日到2020年4月15日招募了17位患者,分别进入不同剂量组:50mg(n=3),100mg(n=3),200mg(n=3),300mg(n=6)和450mg(n=2)。
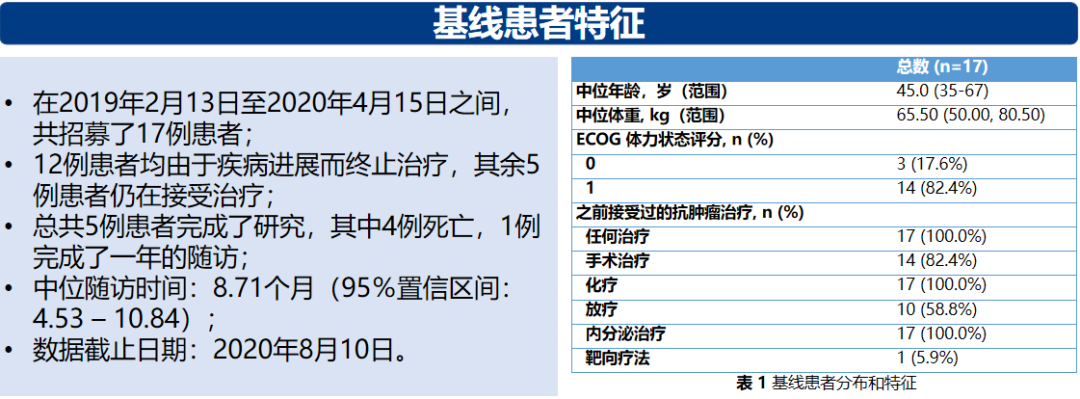
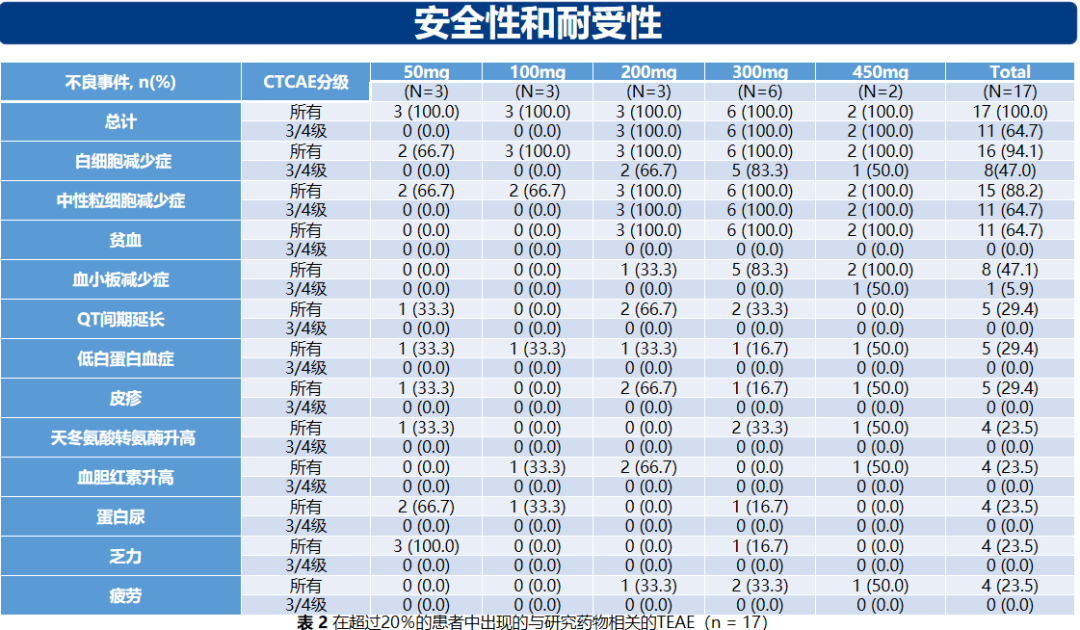
研究结果:截止至2020年8月10日,一共有17例患者参加了1a期临床研究。其中,曾接受内分泌治疗和化疗的患者分别为16例(94.1%)和13例(76.5%)。450 mg剂量组中的两例患者发生了DLT事件,分别为4级血小板减少症和4级中性粒细胞减少症,在其他剂量水平上均未观察到DLT。出现次数最多的是血液学TEAE:白细胞减少症(16/17,94.1%),中性粒细胞减少症(15/17,88.2%),贫血(11/17,64.7%)和血小板减少症(8/17,47.1%)。主要3-4级TEAE为中性粒细胞减少症和白细胞减少症,分别发生于11例(64.7%)和8例(47.1%)例患者中。
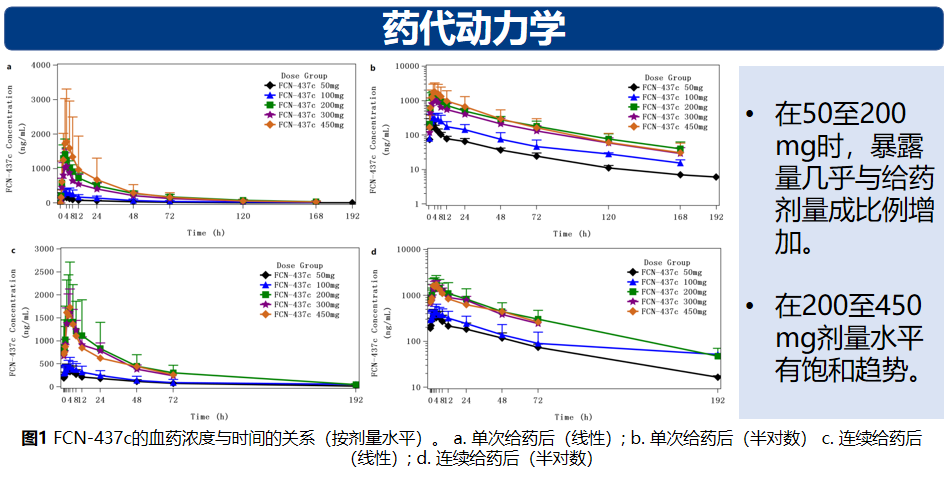
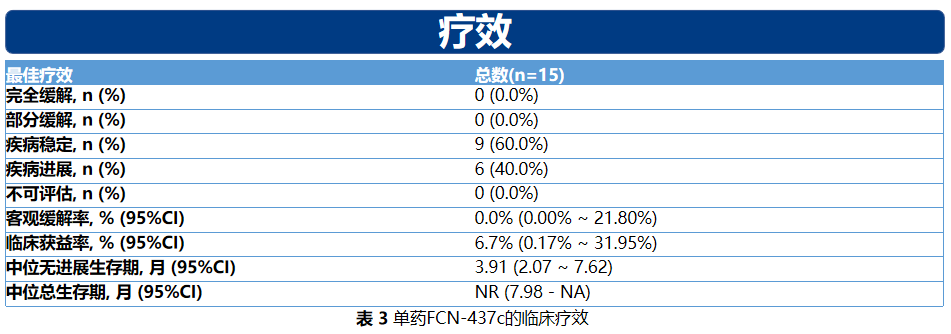
在连续给药50mg到200mg剂量水平中,暴露量(Cmax,AUC0-∞,AUC0-24,Cav-ss 24h)基本与给药量成比例增加。在连续给药200 mg到450 mg剂量水平,暴露量有饱和趋势。FCN-437c单药治疗的MTD确定为300 mg,根据安全性和PK数据将RP2D确定为200 mg。在15例可评估患者中有9例(60.0%)疾病稳定,但未观察到疗效。由于随访时间短,PFS和OS的数据尚未成熟。
研究结论:FCN-437c安全性良好,毒性可耐受。目前FCN-437c在200 mg剂量水平与来曲唑或氟维司群联合治疗初治或复发/难治的ER + HER2-ABC患者的Ⅱ期临床试验正在进行中。
FCN-437c研发情况及研发计划
FCN-437c是一种口服、强效、高选择性、全新结构的CDK4/6 抑制剂,其作用机制在于通过选择性抑制CDK4/6-Cyclin D 二聚体激酶活性,阻碍Rb的磷酸化,阻断细胞从G1期进入S期,使细胞周期停滞于G1期,从而抑制肿瘤细胞的增殖。体内外试验结果证明,在乳腺癌细胞株MCF7等及人乳腺癌MCF7裸小鼠皮下移植瘤模型等中,FCN-437c联合芳香化酶抑制剂或氟维司群具有高效的抗肿瘤活性,与palbociclib和ribociclib相当或更优。FCN-437c具有良好的药代动力学(PK)特性和血脑屏障的渗透性。
目前已经有3项临床研究开展,包括在美国晚期实体瘤患者中开展的1期临床研究FCN-437c-001,中国1期研究AH150201和2期研究AH150202。本次AACR发表是基于AH150201研究的1a期数据,这是一项多中心、开放、单臂剂量探索和剂量扩展的临床研究:评价FCN-437c在ER+、HER2-的晚期乳腺癌女性患者中,单药或联合来曲唑的安全性、耐受性、药代动力学特征、及其抗肿瘤活性。
这个研究在剂量爬坡阶段共入组无标准治疗的复发难治的HR+HER2-晚期乳腺癌17例,采用常规的3+3的剂量爬坡原则,50mg作为起始剂量,最高爬至450mg,采用连续口服治疗3周,休息1周,28天一个周期的给药方式,最终200mg定为2期推荐剂量。整体安全性良好,易管理,主要毒性为骨髓抑制,白细胞减少和中性粒细胞减少是最主要的不良反应,但截至目前未合并发热或感染等不良反应报告,通过支持治疗或短暂停药后可恢复。非血液毒性轻微,绝大多数为1-2级,无3级及以上的QT间期延长、转氨酶升高、腹泻等不良发应报告。其中15例患者已经获得了疗效评估的数据,这些均为高度经治的患者,FCN437单药治疗的疾病控制率达到了60%,由于随访时间短,PFS和OS的数据尚未成熟。
2020年已经开始了对FCN-437c联合来曲唑/氟维司群治疗初治和复发的ER+/HER2-的晚期乳腺癌的探索,初步疗效数据积极,计划于今年下半年开始启动3期临床研究,希望为晚期的乳腺癌患者提供新的治疗选择。
复旦大学附属肿瘤医院肿瘤内科行政副主任
复旦大学附属肿瘤医院一期病房医疗主任
上海市“医苑新星”杰青人才获得者
中国抗癌协会乳腺癌专业委员会常务委员
CSCO乳腺癌专家委员会委员
长江学术带乳腺联盟YBCSG主任委员
上海市抗癌协会肿瘤药物临床研究专业委员会候任主任委员
中国研究型医院协会乳腺专业委员会青委会副主任委员
国家抗肿瘤药物临床应用监测青年专家委员会副主任委员
上海市抗癌协会肿瘤药学专业委员会副主任委员
CSCO肿瘤支持与康复治疗专家委员会常务委员
CSCO青年专家委员会常务委员
国家食品药品监督管理总局CDE首批化药临床兼职审评员
研究申办方:上海复星医药全资子公司锦州奥鸿药业有限责任公司





 京公网安备 11010502033352号
京公网安备 11010502033352号